네이처 자매지인 네이처 커뮤니케이션즈(Nature communications)에 논문 게재
GIST는 공동 연구팀이 단일분자 형광 이미징 기술을 이용해 새로운 크리스퍼 기반 기술들의 핵심 단백질 중 하나인 Cas12a(또는 Cpf1)가 표적 DNA를 탐색하고 절단하는 전 과정을 실시간으로 관찰하는데 성공했다고 지난 7월 24일 밝혔다.
크리스퍼 유전자 가위를 이용한 유전자 교정기술은 유전자 치료, 새로운 식물 육종 개발 등 다양한 분야에 폭넓게 이용 및 빠르게 발전하고 있으며, 대표적으로 Cas9 유전자 가위가 사용되고 있다. 하지만 일반적으로 크리스퍼 유전자 가위는 표적 DNA와 유사한 염기서열을 가진 DNA까지도 자르는 표적이탈효과(off-target) 및 전체 유전체 내 작동가능한 표적이 제한되는 문제 등이 한계로 지적되고 있다.
이러한 기술적 한계를 극복하기 위해 최근에는 다양한 변종 단백질을 발굴 및 개발하여 유전자 교정기술을 향상하고자 노력하고 있다. 그 중에서도 Cas12a 단백질은 Cas9에 비해 표적 특이성이 높다고 알려져 있어 크게 각광받고 있다. 때문에 Cas12a의 상대적으로 높은 표적 특이성을 이해하고 보다 향상된 유전자 가위를 개발하기 위해서는 Cas12a의 표적 탐색 및 절단 메커니즘을 규명하는 연구가 필요하다.
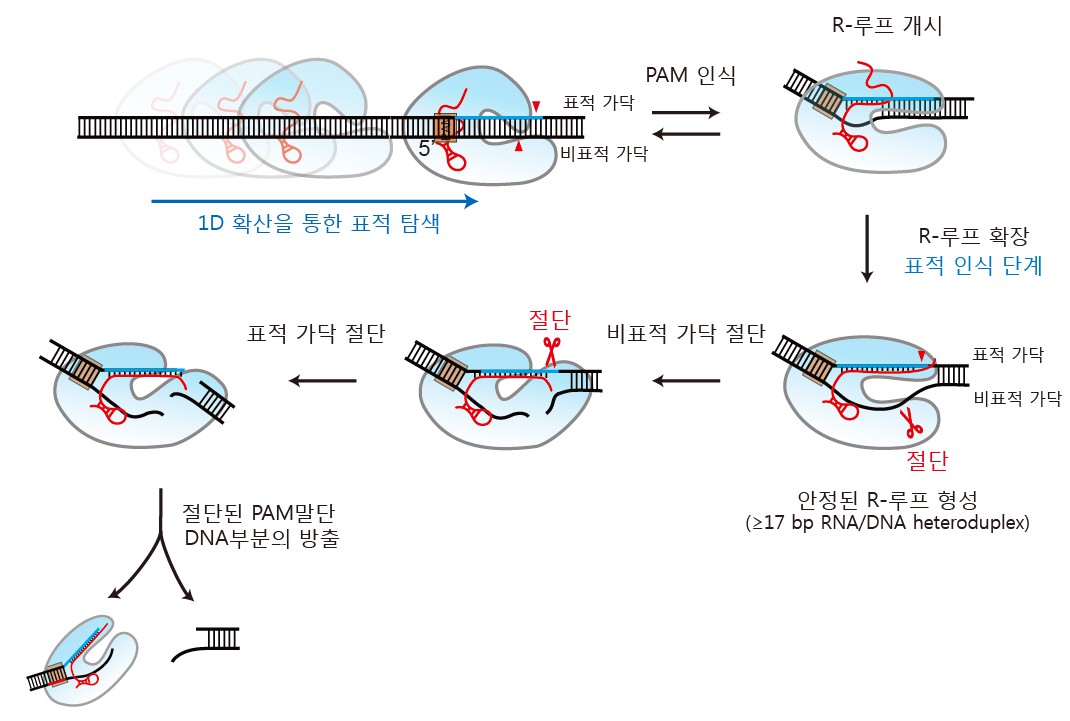
배상수 교수 공동 연구팀은 이번 연구에서 단일분자 형광 이미징 기술을 이용해 Cas12a의 표적 탐색 및 절단의 전 과정을 실시간으로 관찰하는데 성공했다. 이를 통해 Cas12a 단백질이 긴 DNA 상에서 1차원 확산 운동을 통해 특정 표적을 탐색하고, 표적 DNA와 만나 안정된 결합을 한 후, 비표적 가닥과 표적 가닥 순서로 시간 차를 두고 순차적으로 절단한다는 사실을 세계 최초로 규명했다.
배상수 교수(토토사이트 모음대, 공동교신저자), 이상화 박사(GIST, 공동교신저자), 정철현 박사(KIST, 공동교신저자) 등이 주도한 본 연구는 한국연구재단 기초연구사업, 보건복지부 암정복추진연구개발사업, 농촌진흥청 차세대 바이오그린 21사업, GIST 개발과제 및 KIST 기관고유사업 등의 지원을 받아 수행됐으며, 네이처 자매지인 네이처 커뮤니케이션즈(Nature Communications, IF 12.353)에 7월 17일(화) 온라인판에 게재됐다.
관련기사
디지털뉴스팀
hanyang_news@naver.com

 '토토사이트 모음위키' 키워드 보기
'토토사이트 모음위키' 키워드 보기